jac board solutions class 9 science chapter 4 | परमाणु की संरचना | class 9 science chapter 4 question answer
Jac Board Solutions Class 9 Science Chapter 4 : परमाणु की संरचना
सभी अध्यायों के लिए विज्ञान NCERT पुस्तक समाधान Smart Classes के Teachers और Experts के द्वारा बिलकुल आपकी भाषा में तैयार किया गया है | ताकि आप समाधान को समझ सके और आसानी से याद कर सके |
परमाणु की संरचना : Jac Board Solution Class 9 Science Chapter 4
Hindi Medium के लिए कक्षा 9 विज्ञान NCERT समाधान जो की NCERT पुस्तक समाधान नवीनतम CBSE, JACऔर NCERT पाठ्यक्रम पर आधारित है | NCERT पुस्तक समाधान हर साल Smart Classes के द्वारा Update किया जाते है | इसलिए कक्षा 9 के लिए NCERT पुस्तक समाधान भी Smart Classes के द्वारा वर्ष 2022 – 23 के लिए Update किया गया है |
Jac Board Solution Class 9 Science Chapter 4 . Hindi Medium के छात्रों के लिए Hindi में कक्षा 9 विज्ञान NCERT पुस्तक समाधान के सभी अध्याय नवीनतम CBSE, JAC और NCERT पाठ्यक्रम पर आधारित है |
Jac Board Solutions Class 9 Science Chapter 4 : परमाणु की संरचना
Tw Smart Classe , students, teachers, & tutors के requirments के मुताबिक सभी study materials तैयार करती है | हमारे द्वारा और भी study materials तैयार किये जाते है |
हमारे द्वारा तैयार किये गए ncert book solution कुछ इस तरह रहेगी >>
- नोट्स
- अभ्यास
अध्याय 4 : परमाणु की संरचना ( Structure Of the Atom )
♦ इलेक्ट्रान :-
- इलेक्ट्रान की खोज जे. जे. टॉमसन ने किया था
- ये एक ऋणअवेशित कण हे
- इसे e‾ से दर्शाया जाता है |
- इलेक्ट्रोन का द्रव्यमान नगण्य और आवेश – 1 माना जाता है |
- ये परमाणु के कक्षाओं में चक्कर लगाते हें
♦ प्रोटॉन :-
- प्रोटॉन इ गोल्डस्टीन ने किया था |
- ये एक धनअवेशित कण है |
- इसे p+ से दर्शाया जाता है |
- प्रोटॉन का द्रव्यमान 1 इकाई और आवेश +1 लिया जाता है |
- ये परमाणु के नाभिक में मोजूद होता है |
♦ न्यूट्रॉन :-
- न्यूट्रॉन की खोज 1932 में जेम्स चैडविक ने किया था |
- न्यूट्रॉन का कोई आवेश नही होता |
- इसे n से दर्शाया जाता है |
- इसका द्रव्यमान प्रोटॉन के बराबर होता है |
- ये भी परमाणु के नाभिक में मौजूद होता है |
Q1.) केनाल किरने क्या है ?
उत्तर:- 1886 ईo में ई गोल्डस्टीन ने घनावेशित किरण की खोज की जिसका नाम उन्होंने “केनाल किरने” दिया |
Q2.) यदि किसी परमाणु में एक इलेक्ट्रॉन और एक प्रोटॉन है, तो इसमें कोई आवेश होगा या नहीं?
उत्तर:- कोई आवेश नही होगा क्यूंकि प्रोटोन का आवेश +1 इलेक्ट्रोन का आवेश -1 विपरीत तथा बराबर है |
Q3.) जे.जे. टॉमसन का परमाणु मोडल
उत्तर:- जे.जे. टॉमसन के परमाणु मोडल के अनुसार परमाणु एक धन आवेशित गोले का बना होता है जिसमे इलेक्ट्रोन तरबूज के बीज की भांति धंसी होती है |

टॉमसन ने प्रस्तावित किया की –
- परमाणु धन आवेशित गोले का बना होता है और इलेक्ट्रान उसमे धंसे होते है |
- ऋणात्मक और धनात्मक आवेश परिणाम में समान होते हैं | इसीलिए परमाणु वैधुतीय रूप से उदासीन होते है |
Q4.) इ.रदरफोर्ड का परमाणु मोडल
उत्तर:- रदरफोर्ड ने सन 1911 ई० में परमाणु की संरचना का अध्ययन करने के लिए एक प्रयोग किया | इसमें रदरफोर्ड ने रेडिओएक्टिव तत्व पोलेनियम की गतिज उर्जा से निकलने वाली अल्फ़ा – किरणों की एक किरण पुंज को एक बहुत पतले सोने ( स्वर्ण ) के पत्र पर गिराया , तथा फिर देखा की स्वर्ण पत्र में से गुजरते हुए यह अल्फ़ा- कण विभिन्न दिशाओं में विक्षेपित हो जाते है |
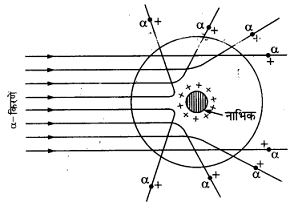
अल्फ़ा- किरणों का इस प्रकार अपने मार्ग से विचलित होने की घटना को प्रकीर्णन कहते है | इस प्रकार रदरफोर्ड के इस प्रयोग को रदरफोर्ड का परमाणु मोडल कहते हैं |
Q5.) नील्स बोर का परमान्विक मोडल
उत्तर:- नील्स बोर के परमान्विक मोडल के अनुसार –
- इलेक्ट्रोन केवल कुछ निशचित कक्षाओं में ही चक्कर लगा सकते हें जिन्हें इलेक्ट्रोन की विविक्त कक्षा कहते हें |
- जब इलेक्ट्रोन इस विविक्त कक्षा में चक्कर लगाते हें तो उनकी उर्जा का विकिरण नही होता है |
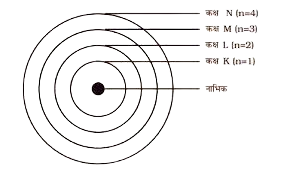
ये कक्षाएं ( कोश ) K , L , M , N . . . . . . . या संख्याओं 1 ,2 ,3 ,4 . . . . . . के द्वारा दिखाई जाती है |
Q1.) पहले अठारह तत्वों के विभिन्न कक्षों में इलेक्ट्रॉन वितरण के नियम को लिखिए।
उत्तर:- इलेक्ट्रॉन वितरण का बोर एवं बरी नियम निम्नलिखित हैं-
(1) किसी कक्ष में अधिकतम इलेक्ट्रॉनों की संख्या 2n² हो सकती है। जबकि n इलेक्ट्रॉन की कक्ष संख्या है।
प्रथम कक्ष में इलेक्ट्रॉन = 2n² = 2 x (1)² = 2
द्वितीय कक्ष में इलेक्ट्रॉन = 2 x (2)² = 2 x 4 = 8
तृतीय कक्ष में इलेक्ट्रॉन = 2 × (3)² = 2 × 9 = 18
(2) बाह्यतम कक्षा में अधिकतम 8 इलेक्ट्रॉन हो सकते हैं। और उससे पहले वाले कक्ष में आधे।
(3) किसी परमाणु के दिए गए कोश में इलेक्ट्रॉन तब तक स्थान नहीं लेते हैं। जब तक कि उससे पहले वाले भीतरी कक्ष पूर्ण रूप से भर नहीं जाते। स्पष्ट होता है कि कक्षाएँ क्रमानुसार भरती हैं।
Q2.) Na के पूरी तरह से भरे हुए K व L कोश होते हैं- व्याख्या कीजिए।
उत्तर:- सोडियम (Na) का परमाणु क्रमांक 11 है; अतः इसका इलेक्ट्रॉनिक विन्यास 2, 8, 1 है। M-कोश के इलेक्ट्रॉन निकल जाने के उपरान्त सोडियम आयन (Na+) प्राप्त होता है जिसके K कोश में 2 तथा L कोश में 8 इलेक्ट्रॉन होते हैं तथा M- कोश विलुप्त हो जाता है। शेष दोनों कोशों में इलेक्ट्रॉनों की संख्या, इन कोशों में होने वाले इलेक्ट्रॉनों की अधिकतम संख्या के बराबर है अर्थात् K तथा L कोश पूर्णतः भरे हुए हैं।
Q3.) निम्नलिखित वक्तव्यों में गलत के लिए- F और सही के लिए T लिखें।
(a) जे. जे. टामसन ने यह प्रस्तावित किया था कि परमाणु के केन्द्रक में केवल न्यूक्लीयॉन्स होते हैं।
(b) एक इलेक्ट्रॉन और प्रोटॉन मिलकर न्यूट्रॉन का निर्माण करते हैं, इसलिए यह अनावेशित होता है।
(c) इलेक्ट्रॉन का द्रव्यमान प्रोटॉन से लगभग 12000 गुणा होता है।
(d) आयोडीन के समस्थानिक का इस्तेमाल टिंक्चर आयोडीन बनाने में होता है। इसका उपयोग दवा के रूप में होता है।
उत्तर:
(a) F
(b) F
(c) T
(d) F
Q4.) रदरफोर्ड का अल्फा कण प्रकीर्णन प्रयोग किसकी खोज के लिए उत्तरदायी था ?
(a) परमाणु केन्द्रक
(b) इलेक्ट्रॉन
(c) प्रोटॉन
(d) न्यूट्रॉन।
उत्तर:
(a) (✓)
(b) (✗)
(c) (✗)
(d) (✗)।
Q5.) एक तत्व के समस्थानिक में होते हैं-
(a) समान भौतिक गुण
(b) भिन्न रासायनिक गुण
(c) न्यूट्रॉनों की अलग-अलग संख्या
(d) भिन्न परमाणु संख्या ।
उत्तर:
(a) (✗)
(b) (✗)
(c) (✓)
(d) (✗)।
Q6.) Cl– आयन में संयोजकता- इलेक्ट्रॉनों की संख्या है-
(a) 16
(b) 8
(c) 17
(d) 18
उत्तर:
(a) (✗)
(b) (✓)
(c) (✗)
(d) (✗)।
Q7.) सोडियम का सही इलेक्ट्रॉनिक विन्यास निम्न में कौन सा है?
(a) 2,8
(b) 8, 2, 1
(c) 2, 1, 8
(d) 2, 8, 1
उत्तर:
(d) 2, 8, 1.
Q8.) कैनाल किरणें क्या हैं?
उत्तर:- र- इलेक्ट्रॉन के सम्बन्ध में जानकारी प्राप्त होने के पहले, ई. गोल्डस्टीन ने 1886 में एक नए विकिरण की खोज की, जिसे उन्होंने ‘कैनाल किरणें नाम दिया। ये किरणें धनावेशित विकिरण थीं, जिसके द्वारा अन्तत: दूसरे अवपरमाणुक कण की खोज हुई।
Q9.) यदि किसी परमाणु में एक इलेक्ट्रॉन और एक प्रोटॉन है, तो इसमें कोई आवेश होगा या नहीं?
उत्तर:- चूँकि एक इलेक्ट्रान और एक प्रोटॉन पर आवेश बराबर होता है, इसलिए एक इलेक्ट्रॉन और एक प्रोटॉन पर आवेश नहीं होगा। दूसरे शब्दों में यह एक उदासीन परमाणु वाली स्थिति है।
Q10.) रदरफोर्ड के परमाणु मॉडल के अनुसार, परमाणु के नाभिक में कौन-सा अवपरमाणुक कण विद्यमान है?
उत्तर:- परमाणु के नाभिक में धनावेशित कण (प्रोटॉन) होता है।
Q11.) क्या अल्फा कणों का प्रकीर्णन प्रयोग सोने के अतिरिक्त दूसरी धातु की पन्नी से सम्भव होगा ?
उत्तर:- सोने की अत्यन्त महीन पन्नी ( लगभग 1000 परमाणुओं के बराबर मोटी) प्राप्त करना सम्भव होता है, जो प्रकीर्णन प्रयोग के लिए आवश्यक है। किसी अन्य धातु की इतनी महीन पन्नी प्राप्त करना सम्भव नहीं है। अतः प्रकीर्णन प्रयोग में सोने के अतिरिक्त किसी अन्य धातु की पन्नी का प्रयोग सम्भव नहीं है।
Q12.) परमाणु के तीन अवपरमाणुक कणों के नाम लिखिए।
उत्तर: परमाणु के तीन अवपरमाणुक कण इलेक्ट्रॉन, प्रोटॉन तथा न्यूट्रॉन हैं।
Q13.) हीलियम परमाणु का परमाणु द्रव्यमान 4u है और उसके नाभिक में दो प्रोटॉन होते हैं। इसमें कितने न्यूट्रॉन होंगे?
उत्तर:- न्यूट्रॉनों की संख्या = परमाणु द्रव्यमान – प्रोटॉनों की संख्या = 4 – 2 = 2
Q14.)कार्बन तथा सोडियम के परमाणुओं के लिए इलेक्ट्रॉन वितरण लिखिए।
उत्तर: कार्बन का परमाणु क्रमांक = 6
इलेक्ट्रॉन वितरण = 2, 4
सोडियम का परमाणु क्रमांक = 11
इलेक्ट्रॉन वितरण = 2, 8, 1
Q15.) अगर किसी परमाणु का K और L कोश भरा है तो उस परमाणु में इलेक्ट्रॉनों की संख्या क्या होगी ?
उत्तर:- K कोश (n = 1) में इलेक्ट्रॉनों की अधिकतम संख्या = 2 (1)2 = 2
L कोश (n = 2) में इलेक्ट्रॉनों की अधिकतम संख्या = 2 (2)2 = 8
अत: परमाणु में 2 + 8 = 10 इलेक्ट्रॉन होंगे |
Q16.) यदि किसी परमाणु में इलेक्ट्रॉनों की संख्या 8 है और प्रोटॉनों की संख्या भी 8 है तब,
(a) परमाणु की परमाणुक संख्या क्या है?
(b) परमाणु का क्या आवेश है?
उत्तर:- (a) परमाणु की परमाणु संख्या परमाणु के नाभिक में उपस्थित प्रोटॉनों की संख्या = 8
(b) चूँकि परमाणुक में इलेक्ट्रॉनों तथा प्रोटॉनों की संख्या समान है| अत: इस पर कोई आवेश नहीं होगा अर्थात् परमाणु विधुत उदासीन होगा।
